- 普瑞基準:多組學技術對于腫瘤創新藥物研發的重要意義
- 2022年06月08日 來源:互聯網
提要:在創新藥研發成功率低、周期長、回報率逐步下降的當前,如何通過現代科技手段破解藥物研發窘境成為業內共識。本文聚焦多組學技術與醫藥創新跨界融合新機遇,南京醫科大學黨委副書記、校長胡志斌,普瑞基準聯合創始人梁晗教授及江蘇品生醫療首席技術官張偉等多位行業專家一起探討了多組學技術的最新成果和在創新藥領域的應用。
在創新藥研發成功率低、周期長、回報率逐步下降的當前,如何通過現代科技手段破解藥物研發窘境成為業內共識。本文聚焦多組學技術與醫藥創新跨界融合新機遇,南京醫科大學黨委副書記、校長胡志斌,普瑞基準聯合創始人梁晗教授及江蘇品生醫療首席技術官張偉等多位行業專家一起探討了多組學技術的最新成果和在創新藥領域的應用。
南京醫科大學黨委副書記、校長胡志斌指出:從隊列研究入手,在創新藥領域,組學數據不僅可以多維度篩選靶點,加速藥物研發進程,還可用于指導疾病分子分型,實現個體化的精準用藥。隨著人類基因組計劃的實施和完成,基因組時代到來。在后基因組時代,芯片和測序技術同樣在快速迭代,不斷催生技術革新和產業升級,高分辨質譜檢測技術、宏基因組等持續完善測序技術。大型多組學隊列資源庫將成為未來原始創新的核心驅動力。
針對國內醫藥研發還存在靶點扎堆、研發同質化的問題,MD Anderson癌癥中心教授、普瑞基準聯合創始人梁晗表示,組學數據的快速積累和數據挖掘技術的進步將為醫藥行業帶來新的窗口期。通過數據挖掘可以輔助企業精準決策,同時也可以通過數據輸出幫助企業制定差異開發策略。
2018年,梁晗教授和Norman Sharpless等科學家受《Cell》邀請發表文章,評論了多組學大數據對于未來癌癥研究和藥物研發的影響,梁晗教授團隊認為,組學數據挖掘正步入癌癥新藥研發的舞臺中央。
過去幾年,梁晗教授團隊研究發現,多組學技術對于腫瘤創新藥物研發的重要意義。在轉錄組領域深入研究了增強子(enhancer)的生物學意義,并且能夠更有效地對免疫治療的效果進行預測;在功能組學方面,建立了高通量的方法,鑒定癌癥驅動基因的新突變、新的融合形式;還針對藥物治療前后的蛋白質差異表達進行了系統研究。
組學大數據的挖掘,可以極大提升新藥研發的效率和決策正確率。在新藥研發核心過程的研究周期從十幾年縮短到幾個月,甚至幾周。同時,基于數據挖掘的決策,能夠避免個體認知偏差,最大化地降低研發風險。

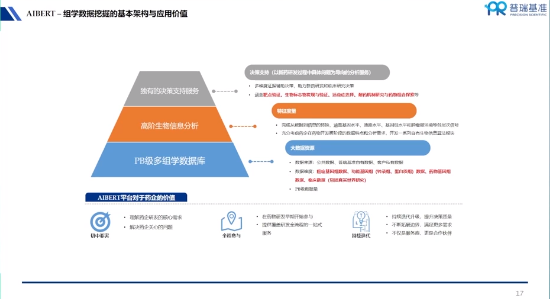
目前,新藥研發企業在海量、高維、異構、不同來源的組學數據整合挖掘并轉化為新藥研發決策能力領域能力稀缺。為了幫助藥企提供新藥研發的差異化開發策略,打造創新管線,普瑞基準多組學數據挖掘系統——AIBERT應運而生。AIBERT包含創新組學試驗平臺和計算平臺,專注于創新靶點發現與評估、適應證選擇、生物標志物發現、耐藥機制研究、藥物聯用方案探索等問題,為藥企提供的支持覆蓋了新藥研發全過程。
在研發早期,藥企能夠提供的樣本規模往往比較小。由于樣本規模小,數據維度高,且變量非常多,會得到很多似是而非的信號,難以甄別。把小樣本數據放在大數據資源背景下,在多個維度上對同一個信號進行反復驗證,找到證據鏈條最堅實的結論,用于指導臨床開發策略。這體現了系統生物學的理念,即不是關注單一基因、單一通路,而是依靠我們整合的PB級別數據資源和生物信息算法(包括深度學習模型),強調對生命復雜系統的整體理解,比如癌癥信號網絡,或者腫瘤微環境系統。
某個在研TKI抑制劑,藥企希望找到其最佳適應癥。一期臨床實驗包括30位患者,17個癌癥類型,平均一個癌種不到兩個患者,決策難度很大。依托AIBERT系統進行深入挖掘,研究者和企業可深入分析一期臨床患者組學數據,找到最佳適應癥,確定藥效相關標志物和抗性標志物。這些結論已經得到藥企驗證并開啟二期臨床試驗。